|
国家药品不良反应监测年度报告 (2023年)
发布日期:2024-03-26
为全面反映2023年我国药品不良反应监测情况,提高安全用药水平,更好地保障公众用药安全,国家药品不良反应监测中心组织编撰《国家药品不良反应监测年度报告(2023年)》。
第1章 药品不良反应监测工作情况
2023年,国家药品不良反应监测中心在国家药品监督管理局的领导下,全面贯彻党的二十大精神,认真落实“四个最严”要求,按照“讲政治、强监管、保安全、促发展、惠民生”的工作思路,扎实有效开展各项工作,为药品监管提供科学有力支撑,切实保护和促进公众健康。 一是体系能力建设纵深推进。贯彻落实《国务院办公厅关于全面加强药品监管能力建设的实施意见》《“十四五”国家药品安全及促进高质量发展规划》,加强对基层监测机构和医疗机构指导,督促药品上市许可持有人(以下简称“持有人”)落实主体责任,持续强化“一体两翼”工作格局。 二是法规制度体系更加完善。配合推进《药品不良反应报告和监测管理办法》修订,研究起草《非处方药转换为处方药工作程序》等技术指南和规范性文件,指导持有人开展药物警戒工作,推动药物警戒制度建立健全。 三是安全风险防控不断加强。密切关注国内外监管动态,强化监测数据分析评价。完成36个(类)药品安全性评价,提出风险控制措施建议,国家药监局发布修订药品说明书公告34期。 四是监测信息系统持续优化。加强基础设施建设,扩容基础环境,增加网络安全防护能力。重构药品不良反应监测系统,推进创新药和附条件批准药品不良反应术语提取信息化建设,为监测评价提供有效技术支撑。 五是监管科学研究深入实施。加强与科研院所、高等院校、医疗机构合作,完成监管科学行动计划第二批重点项目研究。加强重点实验室建设与课题研究,合作开展国家自然科学基金、科技部重大专项课题申报与研究。
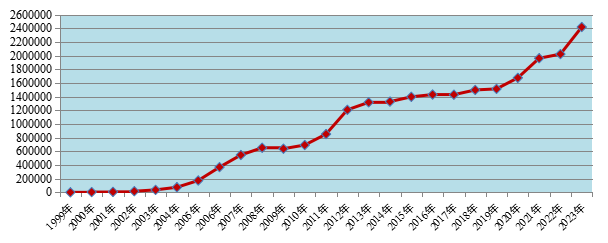
第2章 药品不良反应/事件报告情况 2.1 报告总体情况 2.1.1 2023年度药品不良反应/事件报告情况 2023年全国药品不良反应监测网络收到《药品不良反应/事件报告表》241.9万份。1999年至2023年,全国药品不良反应监测网络累计收到《药品不良反应/事件报告表》2,327.5万份(图1)。
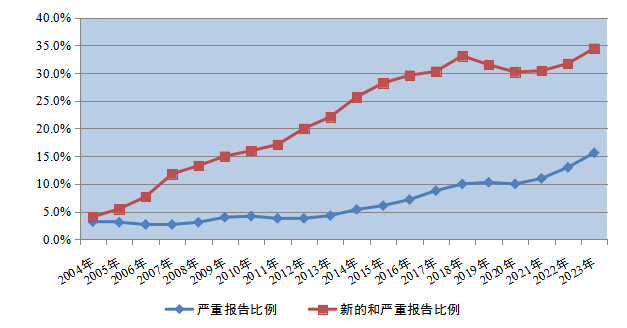
图1 1999年-2023年全国药品不良反应/事件报告数量增长趋势 2.1.2 新的和严重药品不良反应/事件报告情况 2023年全国药品不良反应监测网络收到新的和严重药品不良反应/事件报告83.3万份;新的和严重药品不良反应/事件报告占同期报告总数的34.5%。 2023年全国药品不良反应监测网络收到严重药品不良反应/事件报告37.8万份,严重药品不良反应/事件报告占同期报告总数的15.6%(图2)。 图2 2004年-2023年新的和严重以及严重药品不良反应/事件报告比例
小贴士: 如何正确认识药品不良反应报告? 药品不良反应是指合格药品在正常用法用量下出现的与用药目的无关的有害反应。药品不良反应是药品的固有属性,一般来说,所有药品都会存在或多或少、或轻或重的不良反应。 药品不良反应监测是药品上市后安全监管的重要支撑,其目的是及时发现和控制药品安全风险。持有人、经营企业、医疗机构应当报告所发现的药品不良反应,国家鼓励公民、法人和其他组织报告药品不良反应。 经过各方努力,持有人、经营企业、医疗机构报告药品不良反应的积极性已经逐步提高,我国药品不良反应报告数量稳步增长,与欧盟、美国等国家和地区药品不良反应报告数量发展趋势相同。严重药品不良反应/事件报告比例是衡量报告总体质量和可利用性的重要指标之一,药品不良反应监测评价工作一直将收集和评价新的和严重药品不良反应作为重点内容。新的和严重药品不良反应报告,尤其是严重药品不良反应报告数量增多,并非说明药品安全水平下降,而是意味着监管部门掌握的信息越来越全面,对药品的风险更了解,风险更可控,对药品的评价更加有依据,监管决策更加准确。同样,在医疗实践中,能及时了解药品不良反应发生的表现、程度,并最大限度地加以避免,也是保证患者用药安全的重要措施。
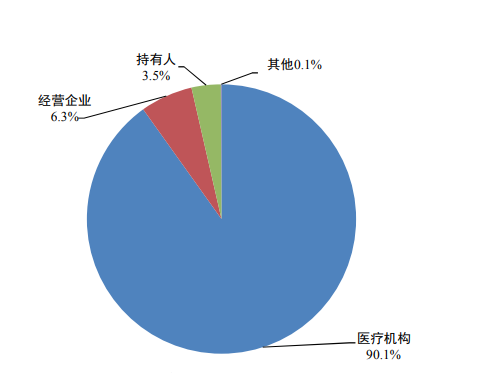
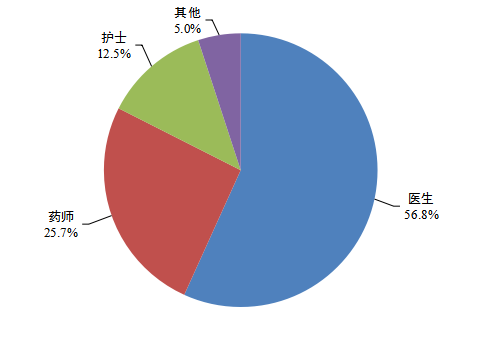
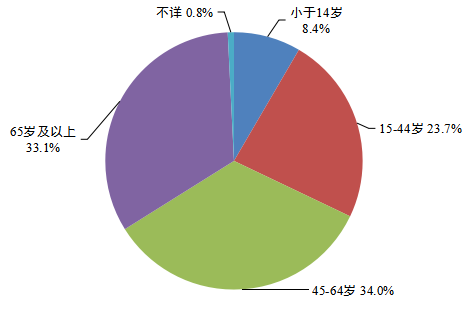
2.1.3 每百万人口平均报告情况 每百万人口平均报告数量是衡量一个国家药品不良反应监测工作水平的重要指标之一。2023年我国每百万人口平均报告数为1,716份。 2.1.4 药品不良反应/事件县级报告比例 药品不良反应/事件县级报告比例是衡量我国药品不良反应监测工作均衡发展及覆盖程度的重要指标之一。2023年全国98.5%的县级地区报告了药品不良反应/事件。 2.1.5 药品不良反应/事件报告来源 持有人、经营企业和医疗机构是药品不良反应报告的责任单位。按照报告来源统计,2023年来自医疗机构的报告占90.1%、来自经营企业的报告占6.3%、来自持有人的报告占3.5%、来自其他报告者的报告占0.1%(图3)。 图3 2023年药品不良反应/事件报告来源 按照报告数量统计,2023年持有人报送药品不良反应/事件报告共计8.5万份,同比增长0.8%。其中,新的和严重药品不良反应/事件报告占持有人报告总数的51.9%,高于总体报告中新的和严重药品不良反应/事件报告占比。 2.1.6 报告人职业 按照报告人职业统计,医生占56.8%、药师占25.7%、护士占12.5%、其他职业占5.0%(图4)。 图4 2023年报告人职业构成 2.1.7 药品不良反应/事件报告涉及患者情况 2023年药品不良反应/事件报告中,女性多于男性,男女性别比为0.84:1。从年龄分布看,14岁及以下儿童患者占8.4%,65岁及以上老年患者占33.1%(图5)。
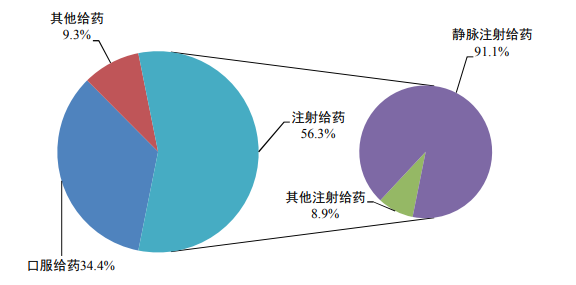
图5 2023年药品不良反应/事件报告涉及患者年龄 2.1.8 药品不良反应/事件报告涉及药品情况 按照怀疑药品类别统计,化学药品占81.2%、中药占12.6%、生物制品占3.8%、无法分类占2.4%(图6)。 图6 2023年药品不良反应/事件报告涉及药品类别 按照给药途径统计,2023年药品不良反应/事件报告中,注射给药占56.3%、口服给药占34.4%、其他给药途径占9.3%;注射给药中,静脉注射给药占91.1%、其他注射给药占8.9%(图7)。
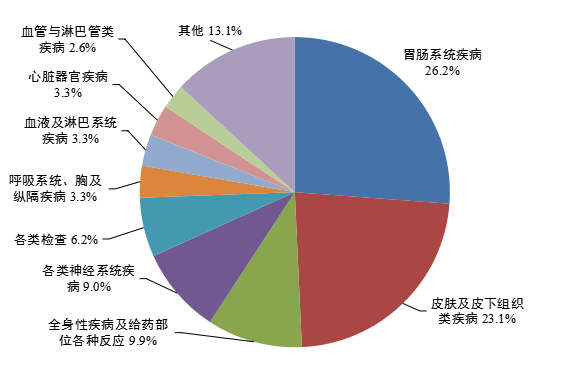
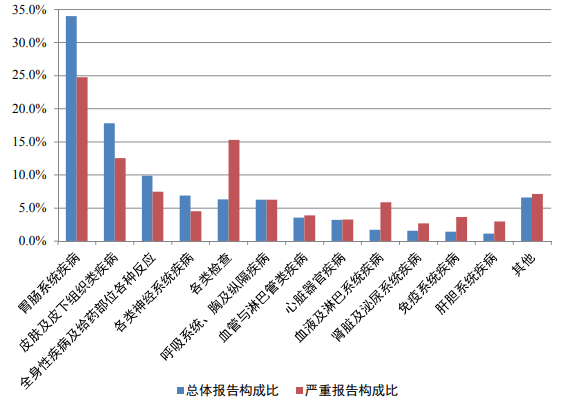
图7 2023年药品不良反应/事件报告涉及给药途径 2.1.9 药品不良反应/事件累及器官系统情况 2023年报告的药品不良反应/事件中,累及器官系统排名前3位依次为胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应(图8)。
图8 2023年药品不良反应/事件累及器官系统 2.2 化学药品、生物制品监测情况 2.2.1 总体情况 2023年药品不良反应/事件报告中,涉及怀疑药品262.7万例次,其中化学药品占81.2%,生物制品占3.8%。2023年严重不良反应/事件报告涉及怀疑药品47.9万例次,其中化学药品占84.9%,生物制品占6.7%。 2.2.2 涉及患者情况 2023年化学药品、生物制品不良反应/事件报告中,男女患者比为0.85:1,女性多于男性。14岁以下儿童患者的报告占8.8%,65岁及以上老年患者的报告占33.4%。 2.2.3 涉及药品情况 2023年药品不良反应/事件报告涉及的化学药品中,例次数排名前5位的类别依次为抗感染药、肿瘤用药、心血管系统用药、镇痛药、电解质/酸碱平衡及营养药。2023年严重药品不良反应/事件涉及化学药品中,报告数量最多的为肿瘤用药,占32.8%;其次是抗感染药,占30.7%。 2023年药品不良反应/事件报告涉及的生物制品中,细胞因子占68.2%、抗毒素及免疫血清占9.0%、血液制品占4.0%、诊断用生物制品占0.3%。 按剂型统计,2023年化学药品不良反应/事件报告中,注射剂、口服制剂所占比例分别为60.8%和32.9%,其他剂型占6.3%。生物制品中,注射剂、口服制剂占比分别为80.1%和1.2%,其他制剂(含不详)占18.7%。 2.2.4 总体情况分析 2023年药品不良反应/事件报告情况与2022年相比未出现显著变化。从不良反应涉及患者年龄看,14岁以下儿童占比出现小幅上升,但总体安全性依然良好;65岁及以上老年患者占比仍然保持升高趋势,提示临床应持续加强对老年患者的安全用药管理。从化学药品类别上看,抗感染药报告数量仍居于首位,其占比在连续多年下降后首次出现上升情况,且莫西沙星和阿奇霉素报告数量出现较大幅度上升,考虑与2023年呼吸道感染性疾病高发有关。生物制品中排名前五位的药品仍以大分子单克隆抗体类抗肿瘤药居多,与2022年相比信迪利单抗、利妥昔单抗的报告数量增幅相对较大。
小贴士: 什么是喹诺酮类药品,使用时应注意什么? 喹诺酮类药品是目前临床常用的抗菌药物,包括左氧氟沙星、莫西沙星、加替沙星、环丙沙星、氟罗沙星、诺氟沙星等。此类药物抗菌谱广,治疗领域宽,临床用量大,不良反应也备受关注。喹诺酮类药品口服或注射均可产生胃肠道反应,如恶心、呕吐、腹痛、腹泻等。因其可通过血脑屏障,还可引起中枢神经系统不良反应,如兴奋、失眠、头痛、头晕、椎体外系反应、幻觉等,严重者出现癫痫大发作、精神分裂样反应、意识障碍等,临床使用时应加强对神经系统不良反应的监测。此类药物还可能影响血糖水平,出现低血糖、高血糖等血糖异常变化,糖尿病患者使用应当格外注意。喹诺酮类药物在尿液中溶解度降低可析出结晶,引起结晶尿、血尿,严重者可导致急性肾功能衰竭,故服药期间应多饮水,每日进水量应在1200 ml以上。一些喹诺酮类还可出现光敏反应,如司帕沙星,使用药物后暴露于紫外线可能发生皮肤痒感、红斑、水肿、水泡等症状,用药期间应注意避光。喹诺酮类药品的其他严重风险,如肌腱炎和肌腱断裂、周围神经病变、主动脉瘤和主动脉夹层等,请参见国家药监局发布的《药品不良反应信息通报》和药品说明书修订公告。
2.3 中药监测情况 2.3.1 总体情况 2023年药品不良反应/事件报告中,涉及怀疑药品262.7万例次,其中中药占12.6%;2023年严重不良反应/事件报告涉及怀疑药品47.9万例次,其中中药占5.4%。 2.3.2 涉及患者情况 2023年中药不良反应/事件报告中,男女患者比为0.8:1,女性多于男性。14岁及以下儿童患者占6.4%,65岁及以上老年患者占31.0%。 2.3.3 涉及药品情况 2023年药品不良反应/事件报告涉及的中药中,例次数排名前5位的类别分别是理血剂中活血化瘀药(20.3%)、清热剂中清热解毒药(13.0%)、祛湿剂中清热除湿药(7.0%)、祛湿剂中祛风胜湿药(4.3%)、补益剂中益气养阴药(3.9%)。2023年中药严重不良反应/事件报告的例次数排名前5位的类别分别是理血剂中活血化瘀药(31.2%)、清热剂中清热解毒药(11.5%)、补益剂中益气养阴药(8.3%)、开窍剂中凉开药(7.1%)、祛湿剂中清热除湿药(4.6%)。 2023年中药不良反应/事件报告中,注射剂和口服制剂所占比例分别为25.9%和60.6%。 2.3.4 总体情况分析 与2022年相比,2023年中药不良反应/事件报告数增长率为17.5%,严重不良反应/事件报告占比为7.6%,低于总体药品不良反应/事件报告中严重不良反应/事件报告占比。从药品类别上看,活血化瘀药的报告数量依然居首位,但占比略有下降。从总体情况看,2023年中药占总体不良反应/事件报告比例呈下降趋势,但仍需要注意安全用药。
小贴士: 为什么中药会引起不良反应? “是药三分毒”,中药和其他药品一样,在发挥治疗作用的同时,也可能会产生一定不良反应。辨证论治是中医认识疾病和治疗疾病的基本原则,严格按照说明书规定的功能主治使用中药,有助于减少和避免不良反应/事件的发生。如果不遵循中医辨证论治的原则或者辨证不当、超说明书功能主治用药,可能增加中药不良反应/事件发生风险。随着中药临床使用日趋广泛,应提高中药安全使用意识。
2.4 基本药物监测情况 2.4.1 国家基本药物监测总体情况 2023年全国药品不良反应监测网络共收到《国家基本药物目录(2018年版)》收载品种的不良反应/事件报告111.2万份,其中严重报告18.9万份,占17.0%。报告涉及化学药品和生物制品占87.9%,中成药占12.1%。 2.4.2 国家基本药物化学药品和生物制品情况分析 《国家基本药物目录(2018年版)》化学药品和生物制品部分共417个(类)品种。2023年全国药品不良反应监测网络共收到国家基本药物化学药品和生物制品药品不良反应/事件报告105.2万例次,其中严重报告21.6万例次,占20.5%。 2023年国家基本药物化学药品和生物制品不良反应/事件报告按照药品类别统计,报告数量排名前5位的分别是抗微生物药、抗肿瘤药、心血管系统用药、激素及影响内分泌药、治疗精神障碍药;累及器官系统排名前5位的是胃肠系统疾病、皮肤及皮下组织类疾病、各类神经系统疾病、全身性疾病及给药部位各种反应、各类检查。 2.4.3 国家基本药物中成药情况分析 《国家基本药物目录(2018年版)》中成药共涉及268个品种。2023年全国药品不良反应监测网络收到国家基本药物中成药不良反应/事件报告14.4万例次,其中严重的不良反应/事件报告11,504例次,占8.0%。2023年国家基本药物7大类中成药中,药品不良反应/事件报告总数由多到少依次为内科用药、骨伤科用药、妇科用药、外科用药、耳鼻喉科用药、儿科用药、眼科用药。 监测数据表明,2023年国家基本药物监测总体情况基本保持平稳。
小贴士: 《国家基本药物目录(2018年版)》收录品种情况 2018年11月1日起,我国正式启用《国家基本药物目录(2018年版)》。该目录主要分为化学药品和生物制品、中成药和中药饮片三个部分。其中化学药品和生物制品部分包括抗微生物药、抗寄生虫病药、麻醉药等26类药品,中成药部分包括内科用药、外科用药、妇科用药等7类药品。与2012年版基本药物目录相比,2018年版基本药物目录共调入药品187种,调出22种(其中17个为化药),目录总品种数量由原来的520种增加到685种,其中西药417种、中成药268种。
第3章 相关风险控制措施
根据2023年药品不良反应监测数据和分析评价结果,国家药品监督管理局对发现存在安全隐患的药品及时采取相应风险控制措施,以保障公众用药安全。 发布胸腺肽注射剂、伊班膦酸钠注射液、卡络磺钠制剂等药品说明书修订公告共34期,增加或完善43个(类)品种说明书中的警示语、不良反应、注意事项、禁忌等安全性信息。 发布《药物警戒快讯》12期,报道国外药品安全信息58条。
第4章 各论
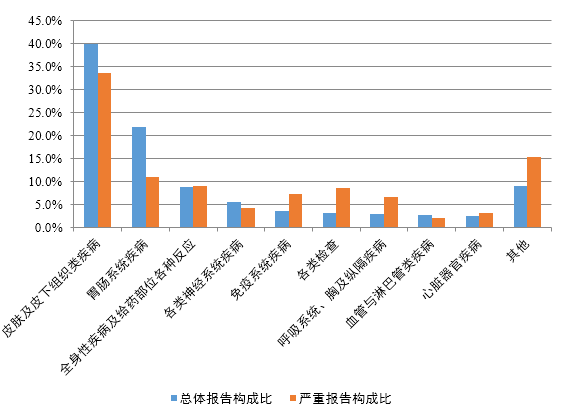
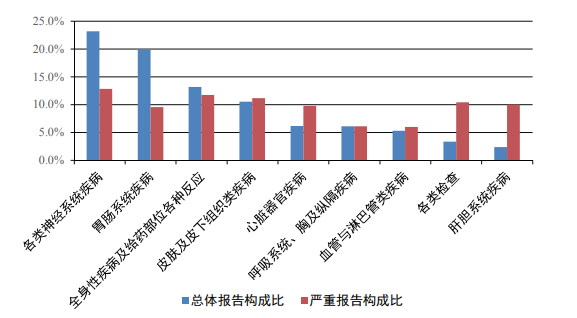
根据药品不良反应监测结果以及公众关注情况,对抗感染药、心血管系统用药、血液系统用药、儿童用药的不良反应报告情况进行分析,并提示安全风险如下。 4.1 抗感染药不良反应监测情况 抗感染药是指具有杀灭或抑制各种病原微生物作用的药品,包括抗生素、合成抗菌药、抗真菌药、抗病毒药等,是临床应用最为广泛的药品类别之一,其不良反应/事件报告数量一直居于首位,是药品不良反应监测工作关注的重点。 2023年全国药品不良反应监测网络共收到抗感染药不良反应/事件报告73.7万份,其中严重报告11.6万份,占15.7%。抗感染药不良反应/事件报告数量占2023年总体报告数量的30.5%。 4.1.1 涉及药品情况 2023年抗感染药不良反应/事件报告数量排名前3位的药品类别分别是头孢菌素类、喹诺酮类、大环内酯类,严重不良反应/事件报告数量排名前3位的药品类别分别是头孢菌素类、喹诺酮类、β-内酰胺酶抑制药。 2023年抗感染药不良反应/事件报告中,注射剂占77.1%、口服制剂占18.5%、其他剂型占4.4%,与药品总体报告剂型分布相比注射剂比例偏高;严重不良反应/事件报告中,注射剂占79.1%、口服制剂占18.4%、其他剂型占2.5%。 4.1.2 累及器官系统情况 2023年抗感染药不良反应/事件报告中,总体报告和严重报告的药品不良反应/事件累及器官系统情况详见图9。与抗感染药的总体报告相比,严重报告的全身性疾病及给药部位各种反应,免疫系统疾病,各类检查,呼吸系统、胸及纵隔疾病,心脏器官疾病构成比偏高。
图9 2023年抗感染药不良反应/事件累及器官系统 抗感染药不良反应/事件报告中,口服制剂累及器官系统排名前5位的是胃肠系统疾病、皮肤及皮下组织类疾病、各类神经系统疾病、肝胆系统疾病、各类检查;注射剂累及器官系统排名前5位是皮肤及皮下组织类疾病、胃肠系统疾病、全身性疾病及给药部位各种反应、各类神经系统疾病、免疫系统疾病。 抗感染药严重药品不良反应/事件报告中,口服制剂累及器官系统排名前5位是皮肤及皮下组织类疾病、肝胆系统疾病、胃肠系统疾病、各类检查、代谢及营养类疾病;注射剂累及器官系统排名前5位是皮肤及皮下组织类疾病、胃肠系统疾病、全身性疾病及给药部位各种反应、免疫系统疾病、各类检查。 4.1.3 监测情况分析及安全风险提示 2023年抗感染药不良反应/事件报告占总体报告比例出现了上升趋势,这可能与2023年流感、肺炎支原体感染等疾病较往年高发以及新冠疫情仍持续一定水平有关。2023年抗感染药严重不良反应报告数量出现了较高的增长,提示抗感染药的用药风险仍需继续关注。
小贴士: 注射用磷霉素钠临床使用时应注意些什么? 注射用磷霉素钠属于广谱抗生素,主要是通过抑制细菌细胞壁的早期合成起到杀菌作用,临床上用于治疗敏感菌所致的各种感染等。接受注射用磷霉素钠治疗的患者有发生严重不良反应的风险,包括高钠血症、低钾血症、过敏性休克、粒细胞缺乏症、肝酶升高等。注射用磷霉素钠静脉滴注速度宜缓慢,每次静脉滴注时间应在1~2小时以上。肝、肾功能减退者慎用,应用较大剂量时应监测肝功能。在开始治疗前应评估高钠血症和水钠潴留的风险,尤其是有充血性心力衰竭病史或伴有肾病综合征、肝硬化、高血压、醛固酮增多症、肺水肿或低蛋白血症的患者。对于接受磷霉素治疗(尤其是长期治疗)的患者,应定期监测其血钠和血钾水平。治疗期间建议低钠饮食,也可以考虑延长输注时长和/或减少单次使用剂量(同时增加给药频次)。磷霉素可能会降低血钾浓度,因此应考虑补钾。
4.2 心血管系统用药不良反应监测情况 心血管系统用药是指用于心脏疾病治疗、血管保护、血压和血脂调节的药品,包括降血压药、抗心绞痛药、血管活性药、抗动脉粥样硬化药、抗心律失常药、强心药等。与2022年相比,心血管系统用药不良反应/事件报告数量同期增长8.7%,严重报告数量同期增长41.2%,提示应对该类药品严重风险给予更多关注。 2023年全国药品不良反应监测网络共收到心血管系统用药的不良反应/事件报告19.0万份,占总体报告的7.9%;其中严重报告1.8万份,占心血管系统用药的9.4%。 4.2.1 涉及药品情况 2023年心血管系统用药不良反应/事件报告数量排名前3位的药品类别是降血压药、抗心绞痛药、血管活性药;心血管系统用药严重报告数量排名前3位的药品类别是抗动脉粥样硬化药、降血压药、抗心绞痛药。 2023年心血管系统用药不良反应/事件报告中,注射剂占27.6%、口服制剂占70.5%、其他剂型占1.9%;严重报告中,注射剂占36.5%、口服制剂占60.1%、其他剂型占3.4%。 4.2.2 累及器官系统情况 2023年心血管系统用药不良反应/事件报告中,总体报告和严重报告的药品不良反应/事件累及器官系统情况详见图10。2023年心血管系统用药不良反应/事件报告中,口服制剂累及器官系统排名前5位是各类神经系统疾病,胃肠系统疾病,全身性疾病及给药部位各种反应,皮肤及皮下组织类疾病,呼吸系统、胸及纵隔疾病;注射剂累及器官系统前5位是各类神经系统疾病、胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应、心脏器官疾病。 2023年心血管系统用药严重不良反应/事件报告中,口服制剂累及器官系统排名前5位的是肝胆系统疾病、各类检查、各类神经系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应;注射剂累及器官系统排名前5位的是全身性疾病及给药部位各种反应、各类神经系统疾病、皮肤及皮下组织类疾病、胃肠系统疾病、心脏器官疾病。
图10 2023年心血管系统用药不良反应/事件累及器官系统 4.2.3 监测情况分析及安全风险提示 2023年心血管系统用药不良反应/事件报告中,降血压药为报告数最多的心血管类药物,这与高血压的治疗药物种类较多有关,还与高血压的发病率较高、用药人群基数大相关。严重不良反应/事件报告中,抗动脉粥样硬化药的报告构成比排名第一,其中阿托伐他汀报告的数量最多;调血脂药的不良反应表现主要为肝功能异常,提示医务人员和患者应关注这类药物的肝损害风险。
小贴士 : 抗动脉粥样硬化药有哪些?使用中应注意什么? 动脉粥样硬化是缺血性心脑血管病的病理基础。在我国,心脑血管病发病率与死亡率近年也明显增加。因而,抗动脉粥样硬化药的使用日益受到关注。常见的抗动脉粥样硬化药主要包括调血脂药、抗氧化药、多烯脂肪酸类及保护动脉内皮药等。调节血脂的药物主要有他汀类,如阿托伐他汀、普伐他汀、辛伐他汀、洛伐他汀、氟伐他汀、瑞舒伐他汀等;以及贝特类、烟酸类等。 他汀类药物是调节血脂异常的首选药物,是很多中老年人长期服用的药物之一。老年人在服用他汀类药物时应关注以下事项:(一)老年患者使用他汀类药物应从小或中等剂量开始,2-3个月后如血脂仍未达标者,患者无肝肾肌酶异常,应调整他汀类药物剂量或种类。服药期间,须规律服药,服用剂量不可随意增大。(二)老年人的生理变化导致肝肾功能减退,常使用多种药物,应关注不同药物间的相互作用,正确选择合并用药,如选择不当,可增加药物的不良反应或降低疗效。(三)注意定期复查,服药2-3月后应复查血脂、肝酶、肌酶及肾功能指标,如果服药期间出现肝脏不适,或肌肉酸痛,无力,褐色尿等症状,应该及时就医。(四)服药期间勿饮西柚汁。西柚中富含的呋喃香豆素可抑制人体内分解药物的酶活性,从而导致进入血液的药量倍增,从而有可能导致药物的毒性反应。除了西柚外,食用柑橘、橙子、柚子等水果也应与药物的服用时间错开。(五)使用他汀类药物使血脂达标后,应坚持长期用药,如无特殊原因不应停药。
4.3血液系统用药不良反应监测情况 血液系统用药主要用于治疗与凝血功能、造血功能、血栓形成以及血容量过低等有关的疾病,包括抗凝血药、促凝血药、促血小板增生药、抗血小板药、抗贫血药、血液成分及血浆代用品、纤维蛋白溶解药、促白细胞药等。 2023年全国药品不良反应监测网络共收到血液系统用药不良反应/事件报告62,422份,其中严重报告12,691份,占20.3%。血液系统用药不良反应/事件报告数量占2023年总体报告数量的2.6%。 4.3.1 涉及药品情况 2023年血液系统用药不良反应/事件报告数量排名前3位的药品类别分别是抗凝血药、促凝血药、抗血小板药,严重不良反应/事件报告数量排名前3位的药品类别分别是抗凝血药、抗血小板药、促凝血药。 2023年血液系统用药不良反应/事件报告中,注射剂占60.0%、口服制剂占37.4%、其他剂型占2.6%,注射剂和口服制剂构成比均高于总体报告;严重不良反应/事件报告中,注射剂占56.2%、口服制剂占39.5%、其他剂型占4.3%。 4.3.2 累及器官系统情况 2023年血液系统用药不良反应/事件报告中,总体报告和严重报告的药品不良反应/事件累及器官系统情况详见图11。与血液系统用药的总体报告相比,严重报告的各类检查、血液及淋巴系统疾病、肾脏及泌尿系统疾病、免疫系统疾病、肝胆系统疾病构成比明显偏高。
图11 2023年血液系统用药不良反应/事件累及器官系统 血液系统用药不良反应/事件总体报告中,口服制剂累及器官系统排名前5位的是胃肠系统疾病,皮肤及皮下组织类疾病,呼吸系统、胸及纵隔疾病,各类检查,全身性疾病及给药部位各种反应;注射剂累及器官系统排名前5位是胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应、各类神经系统疾病、各类检查。 血液系统用药严重药品不良反应/事件报告中,口服制剂累及器官系统排名前5位是胃肠系统疾病,皮肤及皮下组织类疾病,呼吸系统、胸及纵隔疾病,各类检查,全身性疾病及给药部位各种反应;注射剂累及器官系统排名前5位是胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应、各类神经系统疾病、各类检查。 4.3.3 监测情况分析及安全风险提示 近年来,血液系统用药不良反应/事件报告占总体报告比例呈现持续下降趋势,但其严重不良反应报告数量仍然较高,血液系统用药的风险仍需继续关注。
小贴士: 补铁药物临床使用时应注意些什么? 铁剂是一类含有铁元素的药物,主要用于补充人体中铁元素缺乏,治疗缺铁性贫血。临床常用的补铁药物包括无机亚铁盐类(硫酸亚铁)、有机亚铁盐类(琥珀酸亚铁、富马酸亚铁、乳酸亚铁等)、络合铁(蛋白琥珀酸铁、多糖铁等)。这些药物的主要不良反应包括胃肠道反应以及长期大量服用后可能引起铁过载。胃肠道反应的主要表现包括恶心、呕吐、上腹疼痛、便秘黑便等,铁过载主要表现包括肝功能异常、肝硬化、糖尿病、心律失常、心力衰竭、皮肤色素沉着、甲状腺功能减退、不孕症、性功能减退等。络合铁类药物的胃肠道反应最小,有机亚铁盐类次之,硫酸亚铁胃肠道反应最大,餐后服用这些可减少胃肠道反应。缺铁性贫血的治疗至少需要4个月,治疗过程中应定期检查以防止铁过载;此外,应当注意某些中药材是含铁量很高的矿物,如绿矾(主要成分为硫酸亚铁)和代赭石(主要成分为三氧化二铁),含这些药材的中药与西药铁剂联用易出现铁过载。
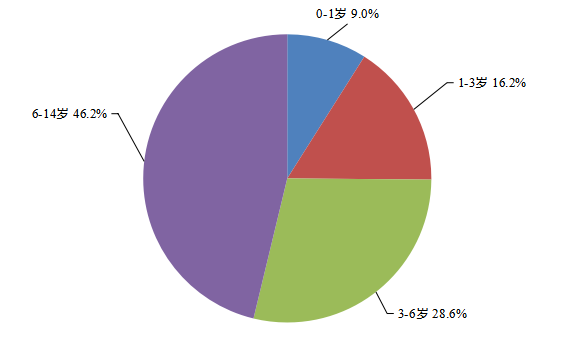
4.4儿童用药监测情况 2023年国家药品不良反应监测网络共收到0-14岁儿童患者报告占总报告数8.4%。儿童患者严重报告占儿童患者总报告数14.1%。 4.4.1 涉及患者情况 2023年儿童患者药品不良反应/事件报告中,男性和女性患儿比例为1.3:1,男性高于女性。2023年儿童患者药品不良反应/事件报告年龄分组情况见图12。
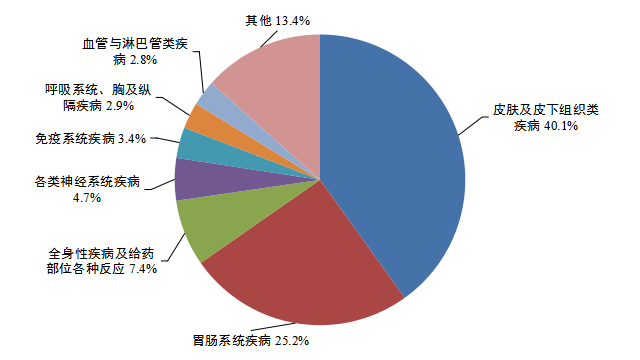
图12 2023年儿童患者药品不良反应/事件报告涉及儿童患者年龄 4.4.2 涉及药品情况 按照药品类别统计,化学药占87.9%、中药占10.0%、生物制品占2.1%。化学药品排名前5位的是抗感染药,电解质、酸碱平衡及营养药,呼吸系统用药,代谢及内分泌系统用药,镇痛药。中药排名前5位的是清热剂、解表剂、止咳平喘剂、祛痰剂、开窍剂。 2023年儿童患者药品不良反应/事件报告中,注射剂占70.4%、口服制剂占21.8%、其他制剂占7.8%;化学药品不良反应/事件报告中,注射剂、口服制剂所占比例分别为75.4%和16.5%。中成药不良反应/事件报告中,注射剂、口服制剂所占比例分别为25.6%和68.3%。生物制品中,注射剂占比例95.2%。 4.4.3 累及器官系统情况 2023年儿童患者药品不良反应/事件报告中,累及系统排名前3位的是皮肤及皮下组织类疾病、胃肠系统疾病、全身性疾病及给药部位各种反应(图13)。化学药累及系统前三位的与总体一致,中成药累及系统排名前三位胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应。生物制品累及系统与整体排序有所差异,以各类检查、全身性损害、皮肤及皮下组织类疾病为主。
图13 2023年儿童患者药品不良反应/事件累及器官系统 4.4.4 监测情况分析及安全风险提示 2023年儿童患者药品不良反应/事件报告占报告总数的8.4%,严重报告占比低于全人群总体情况,总体风险可控。药物治疗是儿童防病治病的主要手段,因儿童生长期的生理特点,对药物具有特殊的反应性和敏感性,因此应持续关注儿童人群用药安全。 2023年统计数据显示,儿童患者用药在药品类别分布上,化学药品与2022年相同,抗感染药,电解质、酸碱平衡及营养药,呼吸系统用药的构成比高于该类别药品在化学药总体报告中的构成比;中药排名居前的药品类别为清热剂、解表剂、止咳平喘剂、祛痰剂,这可能与儿童患者疾病谱使用以上药品较多及生理特点有关。
小贴士: 切莫迷信“网红处方”,儿童用药安全第一。 儿童的生理特点与成人不同,他们的身体发育尚未成熟,对药物的代谢和排泄能力也较弱,因此在使用药物时需要特别小心。 “网红处方”往往是指在网络上广泛传播、备受推崇的某些药物或治疗方案。然而,这些药物或方案并不一定适合每个儿童,甚至可能存在潜在的风险。要注意的是,“是药三分毒”,尤其是儿童用药,如不对症,不仅会延长病程,还可能引起副作用。如果没有按照医嘱或说明书正确使用,当孩子同时服用多种药物,比如含有退热成分的复方感冒药和退热药联合使用时,往往会存在药物过量的风险,甚至会出现肝脏损伤。因此,家长在给孩子用药时,切莫盲目迷信“网红处方”,而应按照说明书使用非处方药,或者遵循医生和药师的建议和指导用药。 为了确保儿童用药安全,家长需要注意以下几点: 遵循医生的医嘱。医生会根据孩子的病情和身体状况开具合适的药物处方,家长应严格按照医生的医嘱给孩子用药,不要自行增减剂量或更改用药方式。 注意药物的副作用。儿童对某些药物的副作用可能更为敏感,家长在给孩子用药时应密切观察孩子的反应,如出现不适症状应及时就医。 尽量减少联合用药。尽量避免给孩子同时使用多种药物,特别是成分相似或作用机制相同的药物,以减少药物相互作用等风险。 注意药物的保存。药品应存放在儿童无法触及的地方,避免孩子误食。同时,家长还应注意药品的保存条件,如避光、防潮等,以确保药品的质量。 总之,儿童用药安全是家长和社会共同关注的重要问题。在给孩子用药时,家长应保持理性,不要盲目追求“网红处方”,而应遵循医生和药师的建议和指导,确保孩子的用药安全。
第5章 有关说明
5.1 本年度报告中的数据来源于国家药品不良反应监测数据库中2023年1月1日至2023年12月31日各地区上报的数据。 5.2 与大多数国家一样,我国药品不良反应报告是通过自发报告系统收集并录入到数据库中的,存在自发报告系统的局限性,如漏报、填写不规范、信息不完善、无法计算不良反应发生率等。 5.3 每种药品不良反应/事件报告的数量受到该药品的使用量和不良反应发生率等诸多因素的影响,故药品不良反应/事件报告数量的多少不直接代表药品不良反应发生率的高低或者严重程度。 5.4 本年度报告完成时,其中一些严重报告、死亡报告尚在调查和评价的过程中,所有统计结果均为现阶段数据收集情况的真实反映,并不代表最终的评价结果。 5.5本年度报告相关医学术语统计采用人用药品技术要求国际协调理事会(ICH)监管活动医学词典(MedDRA)。MedDRA是在ICH主办下编制的标准化国际医学术语集,用于与人用医疗产品相关的监管沟通和数据评估。各类检查是MedDRA中的一项系统器官分类,包括有限定词(例如:升高、降低、异常、正常)和没有限定词的检查名称。 5.6 专业人士会分析药品与不良反应/事件的关联性,提取药品安全性风险信息,根据风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入安全性信息,更新药品如何安全使用的信息等。当药品的获益不再大于风险时,药品也会撤市。 5.7 本年度报告数据均来源于全国药品不良反应监测网络,不包含疫苗不良反应/事件的监测数据。 |
|